|
|
马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?免费注册用户名
×
酷炫化学实验图集:第一弹(●—●) 2015-03-16 [url=]仪器信息网[/url]- l5 N% v' o9 J+ `$ l
; x2 M+ O( ?, I, `' S水火交融
+ m8 E: c0 f/ S) t1 l" L, U/ {: o原理:烧杯底部放入了少量乙醚和金属钾,当加入水时,金属钾与水反应生成氢气并大量产热,造成氢气和乙醚蒸汽的燃烧,而隐约可见的紫色火焰来自钾离子的焰色反应。 Y7 H7 I9 W0 t+ u
花絮:在元素周期表上,越靠下的碱金属性质越活泼,与水的反应也越剧烈。当然,铯才是其中真正的大杀器。
2 Z" Y& O( _, \2 S( y1 d/ A$ c+ y. |3 A; z. @/ H) O& @" R& B
! _( c( P/ v+ F, J! }6 Y% E
红与黑
* V' u! E3 n! M1 u2 V原理:这是“碘钟反应”的一个变种。实验中所用到的三种无色透明溶液(从前到后)分别加入了:可溶性淀粉和焦亚硫酸钠、氯化汞、碘酸钾" g. z: Z" M8 [" w/ j
其中发生的反应包括:
" u- p! g+ n- W5 j$ n9 G( M$ I, \焦亚硫酸钠与水反应生成亚硫酸氢钠 Na2S2O5 + H2O → 2 NaHSO3
) _* z5 ]6 v( W- K" \亚硫酸氢钠将碘酸根还原为碘离子 IO3- + 3HSO3- → I- + 3SO42- + 3H+3 @" w& W2 i7 ~
随着碘离子浓度的升高,可溶性的汞盐开始与碘离子形成碘化汞沉淀(橙红色)Hg2+ + 2 I- → HgI2
! Z/ p1 }9 h0 @! P8 S! E7 x: x剩余的碘离子与碘酸根离子生成碘单质 IO3- + 5I- + 6H+ → 3I2 + 3H2O
) j6 j" G# S6 X2 P0 z碘单质与可溶性淀粉结合形成蓝黑色的包合物
6 X V4 \" j6 u; j% S, U7 Q花絮:因为颜色的缘故,它也被叫做“万圣节反应”。; e3 ]9 Q/ N% K8 T: E) s
; }. ?- D/ e1 D/ ?0 c7 }$ U B
铜和硝酸 - V# ~6 S, R3 ~9 U# u - V# ~6 S, R3 ~9 U# u
原理:铜与浓硝酸反应,生成硝酸铜、二氧化氮和水,生成的气体通入水中,随着气体生成停止并逐渐溶解,水倒吸进入反应瓶,最终形成淡蓝色的硝酸铜溶液。8 b" A0 G( v c+ n2 Z5 P
Cu(s) + 4HNO3(aq) → Cu(NO3)2(aq) + 2NO2(g) + 2H2O(l)
! t4 x( N8 ~9 m" B# D T一开始出现的绿色与浓酸条件下铜离子与硝酸根的结合有关[2],而在引入更多水之后,溶液就显示为水合铜离子的蓝色了。
4 v6 _) L) ]8 ?6 y# a! X' Z花絮:铜和浓硝酸大概是最难背的高中化学反反应了……等等,还有稀硝酸。你还记得怎么配平吗?/ x' x. r7 X* l: J
) I" i$ v- W. e8 `; W- k甲烷泡泡) x* w5 U3 P. ?; {+ E: ]2 N4 ~
 7 x% T$ s+ Q5 Z+ d# ] 7 x% T$ s+ Q5 Z+ d# ]
原理:将甲烷通入肥皂水产生甲烷气泡。在点燃泡泡时,其中的甲烷气体迅速燃烧。
z3 H! R5 P% |花絮:事实上,在自然界也可以找到甲烷泡泡,冬天的时候它们会出现在一些封冻的湖中,这种泡泡也是非常易燃的。" ^& R) d. R9 {: d- P' |+ U0 w6 R
' O3 V8 S& b; w; _+ E
魔法掸子 4 Y; ?: k) o- ` 4 Y; ?: k) o- `
原理:实际上和掸子无关,爆炸的是纸上的物质。三碘化氮是一种可以发生接触爆炸的物质,稍有扰动即可引起爆炸分解,并产生紫色的碘蒸气。/ N: [- D. \6 m! m" J! `
花絮:另一种会发生爆炸性分解的物质是叠氮化钠,它在受撞击时分解产生大量氮气,因此也被用来制作汽车安全气囊。2 F6 A& [" j( _- b
9 }, E( u3 D5 O2 o; D T; M) n! }锂树银花
5 X1 T+ W/ o- [- _( U0 J& G原理:这是金属锂燃烧的景象,燃烧过程中固态的金属锂不断熔化,并生成氧化锂。锂的焰色反应为红色,但当剧烈燃烧时火焰呈现一种“亮银色”的状态。, d: X( k, ~! T
花絮:和其他碱金属一样,锂火不能用水来扑灭,需要专门的干粉灭火剂。
2 f6 M! {# a, |9 S1 ~$ m5 k3 b, V+ M1 i3 {/ ?* q! h
1 M1 a5 e# r1 r( a5 O7 z
小熊糖火山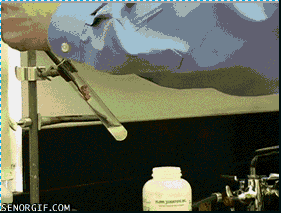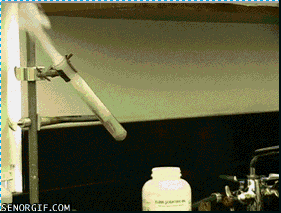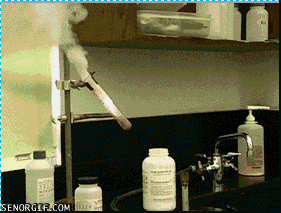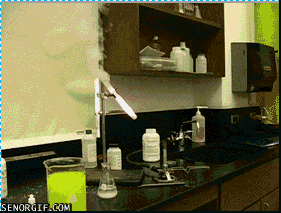 , G# {; Q: [- _+ z5 X , G# {; Q: [- _+ z5 X
原理:试管中是加热到熔融状态的氯酸钾,氯酸钾发生热分解产生氧气,试管中的氧气和热足以点燃小熊软糖中的糖类等有机物。氧气促进燃烧,而燃烧产生的热量又进一步促进氯酸钾分解产生更多氧气,因此就产生了剧烈的燃烧反应。
* k# i* q( i8 l d花絮:这个实验还有一个更加丧心病狂的超大号版本(原视频录制者:Vat19):0 Y4 }) T: g# D2 I( S0 d0 l' M" O

( v( A! G0 c2 Z S录制者:wallsacc
9 w# ^' F9 v9 U危险:高。反应非常剧烈,尤其是超大号版本绝对不建议在家尝试(浪费食物不是好孩子!)。4 e2 v4 v6 p8 z: f* L! @1 g$ T
2 u$ Z9 j% O6 x3 q
9 E9 Z" k& Q' \8 s& f3 {9 O
|
|